由中国科学技术大学(USTC)龚伟民教授领导的研究团队与加州大学洛杉矶分校(UCLA)周正红博士合作,阐明了管形成蛋白的结构作为穿过分枝杆菌外膜的蛋白质运输管。该研究发表在《科学进展》上。
引起结核病的分枝杆菌一直困扰着人类社会,它是单一传染源导致死亡的主要原因。由于厚细胞壁和复杂胶囊层的独特结构,分枝杆菌依赖于专门的蛋白质分泌系统。然而,这些嵌入分枝杆菌细胞包膜内的分泌通道尚未见报道。
在这项研究中,研究人员发现,耻垢分枝杆菌(M.smegmatis)中的结核分枝杆菌Rv3705c及其同源物MSMEG_6251是分枝杆菌包膜中的管形成蛋白(TiME,分别简称为mtTiME和msTiME)。
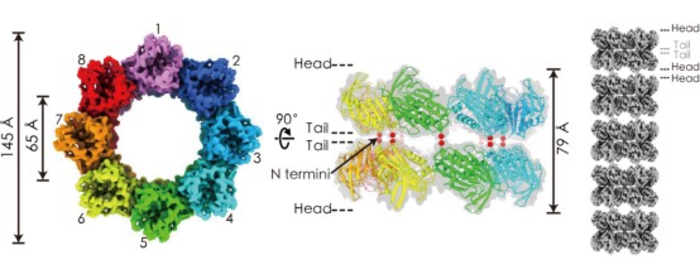
通过结合 X 射线晶体学和冷冻电子显微镜 (cryo-EM),他们发现两种蛋白质形成了内径约 6 nm 的旋转单层环,具有八倍 (C8) 对称性,两层 TiME 环堆积在一起以尾对尾的方式形成一个环形复合体,这些复合体又以头对头的方式堆叠在一起形成管。
此外,体内亚细胞定位结果显示,TiME分布在耻垢分枝杆菌的细胞包膜上,在包膜和细胞壁中的丰度更高,敲除TiME基因后,分子量以下的分泌蛋白量显着减少~在Δmstime培养基中为22 kDa。
在破坏细胞壁的荚膜和表面后,比较野生型和敲除菌株的蛋白质组成,研究人员发现蛋白质的数量没有显着差异,这表明 TiME 形成了跨越分枝杆菌外膜的蛋白质转运通道。
在顶视图(左)和侧视图(中)中由 D8对称性重建的 amphipol 溶解的 mtTiME-FL 的冷冻电镜密度图。双层复合体堆叠的 TiME 管模型(右)。(蔡晓英等人图片)
耻垢分枝杆菌管形成蛋白的鉴定和分析表明,TiME 是分枝杆菌蛋白质分泌的促成因素,为研究病原分枝杆菌的物质转运机制和基于结构的抑制剂设计提供了一种新方法。
